El químico ruso Dimitri Ivánovich Mendeleiev, en 1869, publicó su primera tabla periódica, que contenía 63 elementos. Junto con Lothar Meyer llevaron a cabo la clasificación de acuerdo con los criterios siguientes:
- Colocaron los elementos por orden creciente de sus masas atómicas.
- Situaron en el mismo grupo elementos que tenían propiedades comunes como la valencia.
Una característica de la tabla de Mendeleiev es que deja casillas libres para los elementos por descubrir; el descubrimiento se realizaría años después.
Los trabajos de Moseley relativos al estudio de los espectros de los rayos X de los elementos permitieron conocer el respectivo número atómico. Se comprobó que, al ordenar los elementos según el orden creciente del número atómico, las parejas que resultaban alteradas en la ordenación de Mendeleiev se hallaban incorrectas y de esta forma arregló los errores que existían en la tabla periódica.
Clasificación actual de los elementos
Grupos
Las columnas verticales de la tabla periódica son denominadas grupos. Todos los elementos que pertenecen a un grupo tienen la misma valencia atómica y, por ello, presentan características o propiedades similares entre sí. Por ejemplo, los elementos en el grupo IA tienen valencia 1 (un electrón en su último nivel de energía) y todos tienden a perder ese electrón al enlazarse como iones positivos de +1. Los elementos en el último grupo de la derecha son los gases nobles, los cuales tienen lleno su último nivel de energía (regla del octeto) y, por ello, son todos extremadamente no reactivos. Los grupos que en la tabla llevan números romanos son los grupos A o representativos; los demás son los grupos B o de transición.
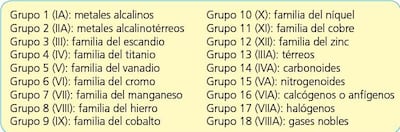
Numerados de izquierda a derecha, los grupos de la tabla periódica son
Periodos
Las filas horizontales de la tabla periódica son llamadas períodos. Contrario a como ocurre en el caso de los grupos de la tabla periódica, los elementos que componen una misma fila tienen propiedades diferentes, pero masas similares: todos los elementos de un período tienen el mismo número de orbitales. Siguiendo esa norma, cada elemento se coloca según su configuración electrónica. El primer período solo tiene dos miembros: hidrógeno y helio; ambos tienen solo el orbital 1s.
La tabla periódica consta de 7 períodos: Periodo 1, Periodo 2, Periodo 3, Periodo 4, Periodo 5, Periodo 6, Periodo 7.
Actividad
Establecé las diferencias entre los criterios de clasificación de los elementos químicos de la tabla propuesta por Mendeleiev y Moseley. Determiná con qué criterio se clasifican actualmente.